熱力学第一法則
0. 熱力学で使われる語句
これがめんどくさい。色々ある。系
とは注目しているものの集まりのこと。準静的
とは無限小の変化を系に加えること。 etc... とまあ色々あってとにかくめんどくさい。やってけば慣れてくか。1. 熱力学第一法則
熱力学第一法則は、エネルギー保存則
である。 なんだかそれっぽい名前がついているのにただこれだけ。簡単ジャン、と思って間違いない。式に表すとこうだ!\[dU = dW + dQ\] Uというのは、系の内部エネルギーのこと。Wは外部から与える仕事。Qは外部から与える熱。dがついているのは、まあ微小な変化を示していると思えば間違いない。つまるところ
(内部エネルギーの変化) = (外から加えた仕事) + (外から加えた熱量)
という、当たり前といえば当たり前の関係式である。ところで、
内部エネルギー
というのは何のエネルギーなのだ、という疑問があった。今のぼくの解釈では、系の持っている全てのタイプのエネルギーを足し合わせたもの、だと思っている。当然、分子の運動エネルギーもだし、たとえばばねの弾性エネルギー、さらには相対論的な質量エネルギーまでも含んでいる、という解釈だ。2. 熱力学における変数
さて、系の状態を表すのに変数は何個必要で、それはどういうものを使えばよいだろうか?そもそも熱力学発端のきっかけは、熱機関(蒸気機関)の解析を理論的に行おうとしたことだった。そこで重要となってくるのが、気体の性質である。蒸気機関は水蒸気のもつエネルギーを仕事に変換するシステムなのだから、そのエネルギー源である水蒸気=気体に興味が出てくる。
気体の状態を表す式としてすぐに思いつくのは、高校で習う
気体の状態方程式
、\[pV = nRT\] だ。pは圧力、Vは体積、nは気体のモル数、Rは気体定数で8.31[J/(molK)]という値、Tは絶対温度である。これからもこの記号を使っていくことにしよう。
状態を表す変数の話に戻る。気体の状態方程式を見る限り、p,V,Tの3つのうち2つが分かれば、他の一つは自動的に決まってしまいそうだ。そこで、熱力学における変数は
p,V,Tの3つのうち2つ
とする。まあとりあえず気体の性質を見るにはこの程度でよいだろうということだ。一般的には、気体の状態方程式として、
\[f(p,V,T) = 0\] の形の式が得られるわけだ。一般論なんか今のところはどうでもいいが。
3. 気体になされる仕事
結局熱力学の中心は気体だ。だったらやっぱり第一法則の中のdWを気体の言葉で表しておくのもよいだろう。いま、下のようなシリンダーに入った気体を考える。
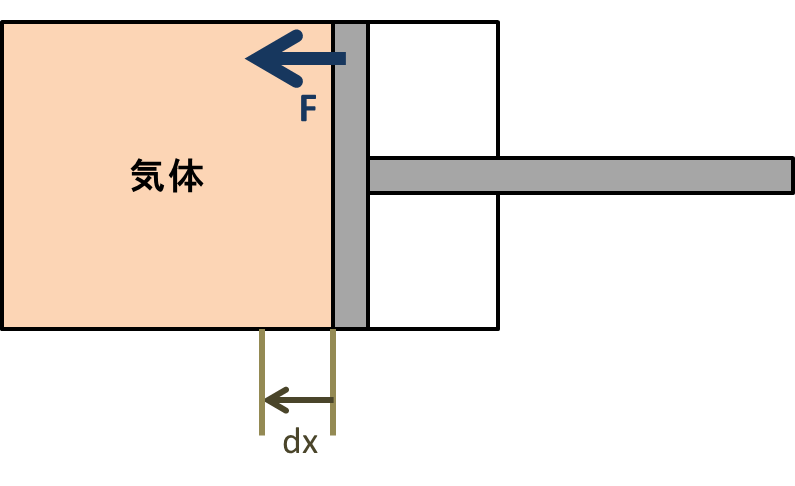
\[dW = Fdx = -(pS)dx = -p(Sdx)\] のように変形することができるだろう。-がついているのは、気体が仕事をしていると解釈してもいい。ここでSdxというのは体積変化とも言うことできる。したがって、一般の場合には、
\[dW = -pdV\] と書くことで対応できる。これによって、熱力学第一法則は下のように書き換えられる。
\[dU = -pdV + dQ\]